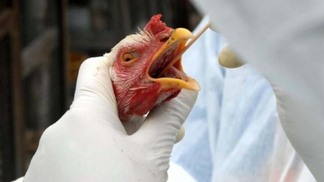
JAMES, J.; WARREN, C.J.; DE SILVA, D.; LEWIS, T.; GRACE, K.; REID, S.M.; FALCHIERI, M.; BROWN, I.H.; BANYARD, A.C. The Role of Airborne Particles in the Epidemiology of Clade 2.3.4.4b H5N1 High Pathogenicity Avian Influenza Virus in Commercial Poultry Production
Units. Viruses, v. 15, n. 1002, 2023. https://doi.org/10.3390/v15041002
Resumo: Desde outubro de 2021, a Europa experimentou a maior epidemia de IA causada
pelo vírus do clado 2.3.4.4b H5N1 AIV de alta patogenicidade (HPAIV), com mais de 284 instalações infectadas por aves domésticas (IPs) e 2.480 aves selvagens H5N1-positivas mortas detectadas somente na Grã-Bretanha.
Muitos IPs se apresentaram como aglomerados geográficos, levantando questões sobre a propagação lateral entre as instalações por partículas transportadas pelo ar.
Transmissão aerógena em curtas distâncias foi observada para algumas cepas de AIV. No entanto, o risco de disseminação pelo ar dessa cepa ainda precisa ser elucidado. Conduzimos ampla amostragem de IPs onde clade 2.3.4.4b H5N1 HPAIVs foram confirmados durante a epidemia 2022/23, cada uma representando uma das principais
espécies de aves (patos, perus e galinhas). Uma série de amostras ambientais foram coletadas dentro e fora dos galpões, incluindo poeira depositada, penas e outros fômites potenciais. O RNA viral (vRNA) e os vírus infecciosos foram detectados em amostras de ar coletadas dentro e fora, mas nas proximidades de casas infectadas, com o vRNA sozinho sendo detectado a distâncias maiores (≤10 m) do lado de fora.
Algumas amostras de poeira coletadas fora das casas afetadas continham vírus infecciosos, enquanto as penas das casas afetadas, localizadas a até 80 m de distância, continha apenas vRNA. Juntos, esses dados sugerem que partículas infecciosas transportadas pelo ar podem ser translocadas a curtas distâncias (<10 m) através do ar, enquanto partículas macroscópicas (gotículas de Flügge – > 2mm de diâmetro) contendo vRNA podem viajar mais longe (≤80 m). Portanto, o potencial de transmissão aerógena do clade 2.3.4.4b H5N1 HPAIV entre instalações é considerado baixo. Outros fatores, incluindo o contato indireto com aves silvestres e a eficiência da biossegurança, representam maior importância na incursão da doença e a eficiência da biossegurança, representam maior importância na incursão da doença.
TRANSMISSÃO DO VIRUS DA IA POR ÁGUAS SUPERFICIAIS, SEDIMENTOS E FEZES DE AVES
Profa. Dra. Masaio Mizuno Ishizuka
Profa. Titular Senior de Epidemiologia das Doenças Infecciosas
AHRENS, A.K.; SELINKA, H.C.; WYLEZICH , C.; WONNEMANN, H.; SINDT, O.; HELLMER, H.H.; PFAFF, F.; HUBERT HÖPER, D.; METTENLEITER, T.C.; BEER, M.; HARDER, T.C. Investigating Environmental Matrices for Use in Avian Influenza Virus Surveillance – Surface Water, Sediments, and Avian Fecal Samples. Microbiology spectrum, v. 11, n. 2, 2023
RESUMO: a vigilância dos vírus da gripe aviária (AIV) em populações de aves aquáticas selvagens é importante para o alerta precoce para proteger as aves de incursões de AIV de alta patogenicidade (HP). O acesso a aves aquáticas individuais é difícil e restrito e limita a profundidade de amostragem.
Aqui, nos concentramos em amostras ambientais, como águas superficiais, sedimentos e fezes frescas de aves depositadas ambientalmente como matrizes para detecção de AIV. O enriquecimento de partículas virais por ultrafiltração de amostras de água de superfície de 10 L usando dispositivos Rexeed-25-A foi validado usando um sistema de controle interno bacteriófago f 6, e a detecção de AIV foi tentada usando RT-PCR em tempo real e
isolamento do vírus.
Enquanto as execuções de validação sugeriram um enriquecimento médio de cerca de 60 vezes, valores mais baixos de 10 a 15 foram observados para amostras de água de campo. No total, 25/36 (60%) das amostras de água superficiais e 18/36 (50%) das amostras de sedimentos correspondentes tiveram resultado positivo para AIV.
As amostras foram obtidas de corpos d’água rasos em habitats com grande número de aves aquáticas durante uma epizootia HPAIV.
Embora o RNA do AIV tenha sido detectado em uma porcentagem substancial das amostras, o isolamento do vírus falhou. As cargas de vírus nas amostras geralmente eram muito baixas para permitir mais sub e patotipagem.
Resultados semelhantes foram obtidos com fezes de aves depositadas no meio ambiente. Além disso, o espectro de vírus detectado por esses métodos de vigilância ativa não refletiu totalmente uma epizootia de HPAIV em andamento entre aves aquáticas detectada por vigilância passiva, que, em termos de sensibilidade, permanece insuperável.